罗莫单抗预装注射器Evenity injection subcutaneous 105mg/1.17mL
[caption id="attachment_18724" align="alignleft" width="300"]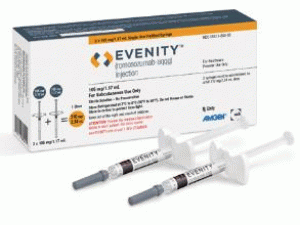
Evenity injection subcutaneous 105mg/1.17mL(罗莫单抗预装注射器)[/caption] 药店国别: 产地国家:美国 处 方 药:是 所属类别:105毫克/17毫升/支 2支/盒 包装规格:105毫克/17毫升/支 2支/盒 计价单位:盒 生产厂家中文参考译名:安进公司 生产厂家英文名:Amgen Inc. 原产地英文商品名:Evenity injection subcutaneous 105mg/1.17mL/syringes 2syringes/box 原产地英文药品名:romosozumab-aqqg 中文参考商品译名:Evenity预装注射器 105毫克/17毫升/支 2支/盒 中文参考药品译名:罗莫单抗-aqqg 曾用名: 简介: EVENITY(romosozumab-aqqg)是第一个也是唯一一个具有双重效果的骨骼生成器,可以增加骨骼训练并减少骨质流失的新药。 近日,美国食品和药物管理局(FDA)批准EVENITY(romosozumab-aqqg)治疗骨质疏松症 绝经后妇女骨折风险高。EVENITY是骨形成的两个原因中的第一个也是唯一一个。EVENITY治疗的全部疗程是由医疗保健提供者每月服用12次.由于骨质疏松症是一种慢性疾病,因此应考虑使用抗再吸收剂继续治疗EVENITY治疗。 批准日期:2019年4月9日 公司:安进公司 EVENITY(罗莫单抗[romosozumab-aqqg])注射液,用于皮下使用 美国最初批准:2019年 警告:心肌病的潜在风险 梗塞,中风和心血管疾病死亡 查看完整的盒装警告的完整处方信息。 •EVENITY可能会增加心肌梗塞,中风和心血管死亡的风险。 •对于在前一年内患有心肌梗塞或卒中的患者,不应启动EVENITY。考虑其他心血管危险因素患者的益处是否超过其风险。 •如果患者在治疗期间出现心肌梗塞或中风,应停止使用EVENITY。 作用机制: EVENITY抑制骨质素的作用,硬化素是骨代谢的调节因子。EVENITY增加骨形成,并在较小程度上减少骨吸收。动物研究表明,thatromosozumab-aqqg通过成骨细胞成骨细胞活动刺激骨小梁和皮质骨表面的骨形成,导致骨生长和皮质骨质量以及骨结构和强度的改善[见非临床毒理学和临床研究]。 适应症和用法: 硬化蛋白抑制剂适用于治疗骨折高风险的绝经后骨质疏松症,定义为骨质疏松性骨折史或多种骨折危险因素;黄金患者已经失败或对其他可用的骨质疏松症治疗不耐受。 使用限制:限制使用12个月剂量的使用时间。如果仍然需要骨质疏松症治疗,应考虑使用抗再吸收剂继续治疗。 剂量和用量: •需要两次单独的皮下注射才能使总剂量达到210mg。一个接一个地注射两个注射器。 •应由医疗保健提供者管理。 每月一次皮下注射210毫克,在腹部,大腿或上臂进行12次剂量。 •治疗期间充分补充钙和维生素D. 剂量形式和强度: 注射:在一次性预装注射器中使用105mg/1.17mL溶液。全新的EVENITY需要两个一次性使用的预充式注射器。 禁忌症: •低钙血症。 •已知对EVENITY过敏。 警告和注意事项: •主要不良心脏事件(MACE):监测MI和中风的症状。 •过敏症:过敏反应,包括血管性水肿,多形性红斑,皮炎,皮疹和荨麻疹。如果发生临床显着的过敏反应,则停止使用。 低钙血症:在使用EVENITY治疗期间充分补充钙和维生素D. •下颌骨坏死:监测症状。考虑基于利益风险评估的治疗。 •非典型股骨骨折:评估新的或不寻常的大腿,臀部或腹股沟疼痛,以排除不完全的股骨骨折。 不良反应: 据报道,最常见的不良反应(≥5%)伴有关节痛和头痛。 用于特定人群: 肾功能损害:严重肾功能不全或发生低钙血症风险较高的患者。监测血清钙,补充钙和维生素D. 包装如何提供/存储和处理 如何提供: EVENITY(romosozumab-aqqg)注射液是一种透明的乳白色,无色至浅黄色的皮下注射溶液,由一次性预装注射器提供。 每个一次性使用的预装注射器含有105毫克EVENITY,可输送体积为1.17毫升。Todeliver有一个全剂量,两剂105mg/1.17ml.EVENEN预充式注射器,一个接一个,总剂量为210mg。 •NDC 55513-880-02:两个105mg/1.17 mL一次性预充式注射器的纸箱。 预装注射器不是用天然橡胶胶乳制成的。 存储和处理: •在原始纸箱中将EVENITY冷却至2°C至8°C(36°F至46°F),以防止光线照射。 不要冻结。 别摇了。 •如果从冰箱中取出,可以将其保存在原始纸箱中最高25°C(77°F)的室温下,并且必须在30天内使用。如果在30天内未使用,请丢弃。 •请勿将EVENITY暴露在高于25°C(77°F)的温度下。 英文说明: EVENITY(romosozumab-aqqg) injection, for subcutaneous use Initial U.S. Approval: 2019 PRINCIPAL DISPLAY PANEL 2x105mg/1.17mL Singe-Use Prefilled Syringe NDC 55513-880-02 EVENITY™(romosozumab-aqqg) injection For Healthcare Provider Use Only 105mg/1.17mL+105mg/1.17 mL=1Dose 210mg/2.34mL 2x105 mg/1.17mL 105mg/1.17mL For Subcutaneous Use Only Sterile Solution – No Preservative Store Refrigerated at 2°C to 8°C (36°F to 46°F).Do not Freeze or Shake. Store in carton to protect from light. Keep out of the sight and reach of children. ATTENTION: Provide the enclose Medication Guide to each patient. For more copies see EVENITY.com or call 1-800-77AMGEN. 2 syringes must be administered fora full 210mg/2.34mL dose

Evenity injection subcutaneous 105mg/1.17mL(罗莫单抗预装注射器)[/caption] 药店国别: 产地国家:美国 处 方 药:是 所属类别:105毫克/17毫升/支 2支/盒 包装规格:105毫克/17毫升/支 2支/盒 计价单位:盒 生产厂家中文参考译名:安进公司 生产厂家英文名:Amgen Inc. 原产地英文商品名:Evenity injection subcutaneous 105mg/1.17mL/syringes 2syringes/box 原产地英文药品名:romosozumab-aqqg 中文参考商品译名:Evenity预装注射器 105毫克/17毫升/支 2支/盒 中文参考药品译名:罗莫单抗-aqqg 曾用名: 简介: EVENITY(romosozumab-aqqg)是第一个也是唯一一个具有双重效果的骨骼生成器,可以增加骨骼训练并减少骨质流失的新药。 近日,美国食品和药物管理局(FDA)批准EVENITY(romosozumab-aqqg)治疗骨质疏松症 绝经后妇女骨折风险高。EVENITY是骨形成的两个原因中的第一个也是唯一一个。EVENITY治疗的全部疗程是由医疗保健提供者每月服用12次.由于骨质疏松症是一种慢性疾病,因此应考虑使用抗再吸收剂继续治疗EVENITY治疗。 批准日期:2019年4月9日 公司:安进公司 EVENITY(罗莫单抗[romosozumab-aqqg])注射液,用于皮下使用 美国最初批准:2019年 警告:心肌病的潜在风险 梗塞,中风和心血管疾病死亡 查看完整的盒装警告的完整处方信息。 •EVENITY可能会增加心肌梗塞,中风和心血管死亡的风险。 •对于在前一年内患有心肌梗塞或卒中的患者,不应启动EVENITY。考虑其他心血管危险因素患者的益处是否超过其风险。 •如果患者在治疗期间出现心肌梗塞或中风,应停止使用EVENITY。 作用机制: EVENITY抑制骨质素的作用,硬化素是骨代谢的调节因子。EVENITY增加骨形成,并在较小程度上减少骨吸收。动物研究表明,thatromosozumab-aqqg通过成骨细胞成骨细胞活动刺激骨小梁和皮质骨表面的骨形成,导致骨生长和皮质骨质量以及骨结构和强度的改善[见非临床毒理学和临床研究]。 适应症和用法: 硬化蛋白抑制剂适用于治疗骨折高风险的绝经后骨质疏松症,定义为骨质疏松性骨折史或多种骨折危险因素;黄金患者已经失败或对其他可用的骨质疏松症治疗不耐受。 使用限制:限制使用12个月剂量的使用时间。如果仍然需要骨质疏松症治疗,应考虑使用抗再吸收剂继续治疗。 剂量和用量: •需要两次单独的皮下注射才能使总剂量达到210mg。一个接一个地注射两个注射器。 •应由医疗保健提供者管理。 每月一次皮下注射210毫克,在腹部,大腿或上臂进行12次剂量。 •治疗期间充分补充钙和维生素D. 剂量形式和强度: 注射:在一次性预装注射器中使用105mg/1.17mL溶液。全新的EVENITY需要两个一次性使用的预充式注射器。 禁忌症: •低钙血症。 •已知对EVENITY过敏。 警告和注意事项: •主要不良心脏事件(MACE):监测MI和中风的症状。 •过敏症:过敏反应,包括血管性水肿,多形性红斑,皮炎,皮疹和荨麻疹。如果发生临床显着的过敏反应,则停止使用。 低钙血症:在使用EVENITY治疗期间充分补充钙和维生素D. •下颌骨坏死:监测症状。考虑基于利益风险评估的治疗。 •非典型股骨骨折:评估新的或不寻常的大腿,臀部或腹股沟疼痛,以排除不完全的股骨骨折。 不良反应: 据报道,最常见的不良反应(≥5%)伴有关节痛和头痛。 用于特定人群: 肾功能损害:严重肾功能不全或发生低钙血症风险较高的患者。监测血清钙,补充钙和维生素D. 包装如何提供/存储和处理 如何提供: EVENITY(romosozumab-aqqg)注射液是一种透明的乳白色,无色至浅黄色的皮下注射溶液,由一次性预装注射器提供。 每个一次性使用的预装注射器含有105毫克EVENITY,可输送体积为1.17毫升。Todeliver有一个全剂量,两剂105mg/1.17ml.EVENEN预充式注射器,一个接一个,总剂量为210mg。 •NDC 55513-880-02:两个105mg/1.17 mL一次性预充式注射器的纸箱。 预装注射器不是用天然橡胶胶乳制成的。 存储和处理: •在原始纸箱中将EVENITY冷却至2°C至8°C(36°F至46°F),以防止光线照射。 不要冻结。 别摇了。 •如果从冰箱中取出,可以将其保存在原始纸箱中最高25°C(77°F)的室温下,并且必须在30天内使用。如果在30天内未使用,请丢弃。 •请勿将EVENITY暴露在高于25°C(77°F)的温度下。 英文说明: EVENITY(romosozumab-aqqg) injection, for subcutaneous use Initial U.S. Approval: 2019 PRINCIPAL DISPLAY PANEL 2x105mg/1.17mL Singe-Use Prefilled Syringe NDC 55513-880-02 EVENITY™(romosozumab-aqqg) injection For Healthcare Provider Use Only 105mg/1.17mL+105mg/1.17 mL=1Dose 210mg/2.34mL 2x105 mg/1.17mL 105mg/1.17mL For Subcutaneous Use Only Sterile Solution – No Preservative Store Refrigerated at 2°C to 8°C (36°F to 46°F).Do not Freeze or Shake. Store in carton to protect from light. Keep out of the sight and reach of children. ATTENTION: Provide the enclose Medication Guide to each patient. For more copies see EVENITY.com or call 1-800-77AMGEN. 2 syringes must be administered fora full 210mg/2.34mL dose
用药温馨提示:当您服用此药物时,需定期接受医疗专业人士的检查,以便随时针对其药效、副作用等情况进行监测。本网站所包含的信息旨在为患者提供帮助,不能代替医学建议和治疗。
药品价格查询,专业药品查询网站,药品说明书查询,药品比价 » 罗莫单抗预装注射器Evenity injection subcutaneous 105mg/1.17mL
药品价格查询,专业药品查询网站,药品说明书查询,药品比价 » 罗莫单抗预装注射器Evenity injection subcutaneous 105mg/1.17mL