前列腺癌如何进行免疫检查点抑制剂治疗
下一代测序可识别可能受益于免疫检查点抑制剂的亚型。
在过去的十年中,免疫检查点抑制剂(CPIs)的使用已改变了癌症的治疗方法,但是尽管有许多临床试验,前列腺癌仍未加入免疫疗法的革命。最近,在恩杂鲁胺(Xtandi)(NCT03016312)中添加的atezolizumab(Tecentriq)的IMbassador 250研究表明,添加atezolizumab无益处。
 很明显,大多数前列腺癌患者无法从当前的CPI中受益,但是很明显,可以通过基因组检测确定可以从免疫疗法中受益的转移性去势抵抗性前列腺癌(mCRPC)的某些分子亚型。我们有许多好的新疗法可以治疗前列腺癌,但转移性疾病仍然无法治愈,将成为大多数患者的死亡原因。他们将死于前列腺癌,而不仅仅是死于前列腺癌。只要这仍然是对的,对前列腺癌的免疫疗法的兴趣仍然很高。
尽管对此的理想答案是让患者参加临床试验,但在某些情况下,非审判治疗是最佳的选择。接下来是我们对晚期前列腺癌患者的CPI评估方法。
下一代测序的作用
前列腺癌患者存在基因表达谱以及种系和体细胞突变的生物学差异。美国国家综合癌症网络指南现在建议对所有患有高危,极高危或转移性前列腺癌的男性进行种系检测。我们还对所有转移性疾病患者进行体细胞(肿瘤)检测,并在系统治疗的基础上,每当病情发展时进行重新检测。
基因组谱分析与下一代测序技术(NGS)的采用已证明,在转移性前列腺癌男性患者的肿瘤中存在多种多样的突变模式。1,2遗传测试可以确定哪些患者可以从PPAR抑制剂中受益,例如olaparib(Lynparza)和rucaparib(Rubraca),还可以确定其肿瘤对CPI更有反应的患者。这些亚型具有与DNA修复缺陷相关的突变3的共同特征,包括缺陷错配修复基因(dMMR)/高微卫星不稳定性(MSI-H),PD-1 T细胞受体及其配体(PD- L1),高肿瘤突变负担(TMB)和CDK12突变的肿瘤。
尽管CPI对普通患者的毒性比化疗低,但在许多研究中,它们并不具有良性,并且与治疗相关的死亡风险很小,但却是真正的风险,并且住院风险为10%到20%。它们也是昂贵的疗法,必须静脉注射(IV)。但是,我们认为应该慎重考虑何时和向谁推荐CPI (表),并将它们限制在基因组学表明有有意义的反应机会的患者中。
对CPI有反应的前列腺癌亚型
dMMR / MSI-H。与没有此类MMR缺陷的肿瘤相比,缺乏dMMR机制的肿瘤发生了超突变,并且来自这些其他突变的新抗原具有更高的免疫原性。鼓励使用NGS在所有晚期前列腺癌患者中寻找dMMR / MSI-H。Pembrolizumab(Keytruda)已获得FDA的全面批准,可用于在先前治疗中进展的dMMR / MSI-H前列腺癌患者。5一项在mCRPC中的初步研究表明,用培姆单抗和enzalutamide组合治疗的dMMR / MSI-H患者的临床反应,表明高的新抗原负荷可以预测对CPI的反应。
在随后的针对mCRPC的病例系列中,只有3.1%(32例患者)患有dMMR / MSI-H PC。在接受PD-1 / PD-L1治疗的11例患者中,有55%的前列腺特异性抗原(PSA)下降,而45%的患者可获得长达19个月的持久临床获益。
很明显,大多数前列腺癌患者无法从当前的CPI中受益,但是很明显,可以通过基因组检测确定可以从免疫疗法中受益的转移性去势抵抗性前列腺癌(mCRPC)的某些分子亚型。我们有许多好的新疗法可以治疗前列腺癌,但转移性疾病仍然无法治愈,将成为大多数患者的死亡原因。他们将死于前列腺癌,而不仅仅是死于前列腺癌。只要这仍然是对的,对前列腺癌的免疫疗法的兴趣仍然很高。
尽管对此的理想答案是让患者参加临床试验,但在某些情况下,非审判治疗是最佳的选择。接下来是我们对晚期前列腺癌患者的CPI评估方法。
下一代测序的作用
前列腺癌患者存在基因表达谱以及种系和体细胞突变的生物学差异。美国国家综合癌症网络指南现在建议对所有患有高危,极高危或转移性前列腺癌的男性进行种系检测。我们还对所有转移性疾病患者进行体细胞(肿瘤)检测,并在系统治疗的基础上,每当病情发展时进行重新检测。
基因组谱分析与下一代测序技术(NGS)的采用已证明,在转移性前列腺癌男性患者的肿瘤中存在多种多样的突变模式。1,2遗传测试可以确定哪些患者可以从PPAR抑制剂中受益,例如olaparib(Lynparza)和rucaparib(Rubraca),还可以确定其肿瘤对CPI更有反应的患者。这些亚型具有与DNA修复缺陷相关的突变3的共同特征,包括缺陷错配修复基因(dMMR)/高微卫星不稳定性(MSI-H),PD-1 T细胞受体及其配体(PD- L1),高肿瘤突变负担(TMB)和CDK12突变的肿瘤。
尽管CPI对普通患者的毒性比化疗低,但在许多研究中,它们并不具有良性,并且与治疗相关的死亡风险很小,但却是真正的风险,并且住院风险为10%到20%。它们也是昂贵的疗法,必须静脉注射(IV)。但是,我们认为应该慎重考虑何时和向谁推荐CPI (表),并将它们限制在基因组学表明有有意义的反应机会的患者中。
对CPI有反应的前列腺癌亚型
dMMR / MSI-H。与没有此类MMR缺陷的肿瘤相比,缺乏dMMR机制的肿瘤发生了超突变,并且来自这些其他突变的新抗原具有更高的免疫原性。鼓励使用NGS在所有晚期前列腺癌患者中寻找dMMR / MSI-H。Pembrolizumab(Keytruda)已获得FDA的全面批准,可用于在先前治疗中进展的dMMR / MSI-H前列腺癌患者。5一项在mCRPC中的初步研究表明,用培姆单抗和enzalutamide组合治疗的dMMR / MSI-H患者的临床反应,表明高的新抗原负荷可以预测对CPI的反应。
在随后的针对mCRPC的病例系列中,只有3.1%(32例患者)患有dMMR / MSI-H PC。在接受PD-1 / PD-L1治疗的11例患者中,有55%的前列腺特异性抗原(PSA)下降,而45%的患者可获得长达19个月的持久临床获益。
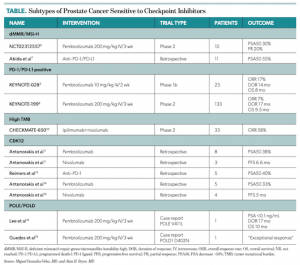 PD-1 / PD-L1的过表达。开放标签的篮子1b期KEYNOTE-028试验每24周研究一次10毫克/公斤的派姆单抗静脉注射,持续24个月。其中包括245例mCRPC患者。PD-L1阳性35例(14%)。在接受Pembrolizumab的PD-L1阳性的35名患者中,有23名患者的总缓解率(ORR)为17%,其中稳定疾病的比例为35%,进行性疾病的比例为39%,中位缓解时间为13.5个月,中位总生存期为8个月。这些发现得到了KEYNOTE-199的确认,这是一项539期多西他赛难治性mCRPC患者每3周使用pembrolizumab 200 mg IV进行为期21个周期的2期试验。8该研究显示PD-L1在mCRPC中的过表达为32%,在8%中在原发性前列腺癌中。8在包括133名患者的PD-L1阳性队列中,ORR为7%,中位缓解时间(mDOR)为16.8个月,完全缓解(CR)为2位患者,中位总生存时间为9.5个月。
值得注意的是,探索PD-1 / PD-L1在前列腺癌中表达的研究使用了不同的技术和阈值,从而导致阳性率的高度可变。总而言之,这些综合结果表明,多达32%的晚期前列腺癌可能使用PD-L1途径逃避了免疫系统的检测。患有mCRPC和PD-L1亚型的患者可从单药pembrolizumab获得少量但有意义的且有时持久的获益。
高TMB。与病程较早的患者相比,mCRPC患者的TMB似乎更高。通常,具有较高TMB的肿瘤与dMMR相关。来自CHECKMATE 650试验(NCT029855957)的初步报告,使用ipilimumab(Yervoy)和nivolumab(Opdivo)联合使用,在TMB高的患者相比TMB低的患者(未报道TMB截止)。结果显示,未进行过化学疗法(60%对0%)和基于紫杉烷的化学疗法(50%对0%)后的ORR均为58%。
双等位基因CDK12突变。CDK12是一种涉及基因组稳定性的肿瘤抑制蛋白。10临床前研究表明,双等位基因CDK12突变与更高的新抗原,肿瘤浸润的淋巴细胞以及对CPI的更高敏感性有关。12,13最初的一项回顾性研究表明,在接受PD-1抑制剂作为四线至六线治疗的8例患者中,CPI敏感性较高。这些经过严格治疗的患者的PSA下降38%,超过50%,中位PFS为6.6个月。14这些结果在一项回顾性研究中得到了证实,该研究涉及46名CDK12患者突变(34个双等位基因突变)。在接受PD-1抑制剂治疗的5名患者中,有40%达到了PSA反应。
最后,一项较大的回顾性多中心研究包括60例患有体细胞功能丧失CDK12突变的前列腺癌患者。9例患者接受了PD-1抑制剂治疗(第5线至第6线使用PD-1抑制剂(5例使用pembrolizumab,4例使用nivolumab),其中33%的患者有PSA反应,中位PFS为5.4个月。16一项正在进行的前瞻性临床试验(NCT03570619)正在研究CDK12作为CPI在前列腺癌中使用的生物标志物的预测作用。
POLE和POLD突变。选择的POLE和POLD突变可产生与无MSI-H的很高TMB相关的肿瘤。在约2%的前列腺癌中发现了这些突变。已有报道,在对Pembrrolizumab的特殊应答者中有病例报告,其中记载了POLE V411L突变。同样,据报道,患有POLD1 D402N,MSH2突变和高TMB的患者对pembrolizumab的临床反应良好。
结论:
在我们的实践中,我们根据患者的肿瘤遗传特征积极地将患者分类到不同的治疗途径上。一小部分但有意义的患者将具有遗传畸变,这些遗传畸变可预测对CPI的反应,而那些幸运患者的结果可能是惊人的。我们尝试让患者尽可能多地参加免疫疗法试验。这些试验通常涉及现有药物的组合,但也可能涉及对mCRPC更有效的全新药物。
我们最近报道了对PT-112进行1期研究的中位先期治疗中位数为6.5行的患者的结果。在该试验中,接受PT-112治疗的10名患者的平均总生存期为15.1个月。我们也将PT-112与avelumab(Bavencio)结合使用,并据此进行研究。
有许多可能性尚待探索,我们需要找到一种将免疫疗法扩展到所有mCRPC患者的方法。同时,NGS可以识别最可能对CPI产生反应的患者,同时还可以识别携带遗传易感基因的患者和将从PARP抑制剂中获益的患者。
Gonzalez-Velez是亚利桑那州凤凰城梅奥诊所的血液学/肿瘤学研究员,而Bryce是亚利桑那州凤凰城梅奥诊所的医学副教授。
相关阅读你推荐:《免疫药联合奥拉帕尼能治疗前列腺癌吗?》
PD-1 / PD-L1的过表达。开放标签的篮子1b期KEYNOTE-028试验每24周研究一次10毫克/公斤的派姆单抗静脉注射,持续24个月。其中包括245例mCRPC患者。PD-L1阳性35例(14%)。在接受Pembrolizumab的PD-L1阳性的35名患者中,有23名患者的总缓解率(ORR)为17%,其中稳定疾病的比例为35%,进行性疾病的比例为39%,中位缓解时间为13.5个月,中位总生存期为8个月。这些发现得到了KEYNOTE-199的确认,这是一项539期多西他赛难治性mCRPC患者每3周使用pembrolizumab 200 mg IV进行为期21个周期的2期试验。8该研究显示PD-L1在mCRPC中的过表达为32%,在8%中在原发性前列腺癌中。8在包括133名患者的PD-L1阳性队列中,ORR为7%,中位缓解时间(mDOR)为16.8个月,完全缓解(CR)为2位患者,中位总生存时间为9.5个月。
值得注意的是,探索PD-1 / PD-L1在前列腺癌中表达的研究使用了不同的技术和阈值,从而导致阳性率的高度可变。总而言之,这些综合结果表明,多达32%的晚期前列腺癌可能使用PD-L1途径逃避了免疫系统的检测。患有mCRPC和PD-L1亚型的患者可从单药pembrolizumab获得少量但有意义的且有时持久的获益。
高TMB。与病程较早的患者相比,mCRPC患者的TMB似乎更高。通常,具有较高TMB的肿瘤与dMMR相关。来自CHECKMATE 650试验(NCT029855957)的初步报告,使用ipilimumab(Yervoy)和nivolumab(Opdivo)联合使用,在TMB高的患者相比TMB低的患者(未报道TMB截止)。结果显示,未进行过化学疗法(60%对0%)和基于紫杉烷的化学疗法(50%对0%)后的ORR均为58%。
双等位基因CDK12突变。CDK12是一种涉及基因组稳定性的肿瘤抑制蛋白。10临床前研究表明,双等位基因CDK12突变与更高的新抗原,肿瘤浸润的淋巴细胞以及对CPI的更高敏感性有关。12,13最初的一项回顾性研究表明,在接受PD-1抑制剂作为四线至六线治疗的8例患者中,CPI敏感性较高。这些经过严格治疗的患者的PSA下降38%,超过50%,中位PFS为6.6个月。14这些结果在一项回顾性研究中得到了证实,该研究涉及46名CDK12患者突变(34个双等位基因突变)。在接受PD-1抑制剂治疗的5名患者中,有40%达到了PSA反应。
最后,一项较大的回顾性多中心研究包括60例患有体细胞功能丧失CDK12突变的前列腺癌患者。9例患者接受了PD-1抑制剂治疗(第5线至第6线使用PD-1抑制剂(5例使用pembrolizumab,4例使用nivolumab),其中33%的患者有PSA反应,中位PFS为5.4个月。16一项正在进行的前瞻性临床试验(NCT03570619)正在研究CDK12作为CPI在前列腺癌中使用的生物标志物的预测作用。
POLE和POLD突变。选择的POLE和POLD突变可产生与无MSI-H的很高TMB相关的肿瘤。在约2%的前列腺癌中发现了这些突变。已有报道,在对Pembrrolizumab的特殊应答者中有病例报告,其中记载了POLE V411L突变。同样,据报道,患有POLD1 D402N,MSH2突变和高TMB的患者对pembrolizumab的临床反应良好。
结论:
在我们的实践中,我们根据患者的肿瘤遗传特征积极地将患者分类到不同的治疗途径上。一小部分但有意义的患者将具有遗传畸变,这些遗传畸变可预测对CPI的反应,而那些幸运患者的结果可能是惊人的。我们尝试让患者尽可能多地参加免疫疗法试验。这些试验通常涉及现有药物的组合,但也可能涉及对mCRPC更有效的全新药物。
我们最近报道了对PT-112进行1期研究的中位先期治疗中位数为6.5行的患者的结果。在该试验中,接受PT-112治疗的10名患者的平均总生存期为15.1个月。我们也将PT-112与avelumab(Bavencio)结合使用,并据此进行研究。
有许多可能性尚待探索,我们需要找到一种将免疫疗法扩展到所有mCRPC患者的方法。同时,NGS可以识别最可能对CPI产生反应的患者,同时还可以识别携带遗传易感基因的患者和将从PARP抑制剂中获益的患者。
Gonzalez-Velez是亚利桑那州凤凰城梅奥诊所的血液学/肿瘤学研究员,而Bryce是亚利桑那州凤凰城梅奥诊所的医学副教授。
相关阅读你推荐:《免疫药联合奥拉帕尼能治疗前列腺癌吗?》
 很明显,大多数前列腺癌患者无法从当前的CPI中受益,但是很明显,可以通过基因组检测确定可以从免疫疗法中受益的转移性去势抵抗性前列腺癌(mCRPC)的某些分子亚型。我们有许多好的新疗法可以治疗前列腺癌,但转移性疾病仍然无法治愈,将成为大多数患者的死亡原因。他们将死于前列腺癌,而不仅仅是死于前列腺癌。只要这仍然是对的,对前列腺癌的免疫疗法的兴趣仍然很高。
尽管对此的理想答案是让患者参加临床试验,但在某些情况下,非审判治疗是最佳的选择。接下来是我们对晚期前列腺癌患者的CPI评估方法。
下一代测序的作用
前列腺癌患者存在基因表达谱以及种系和体细胞突变的生物学差异。美国国家综合癌症网络指南现在建议对所有患有高危,极高危或转移性前列腺癌的男性进行种系检测。我们还对所有转移性疾病患者进行体细胞(肿瘤)检测,并在系统治疗的基础上,每当病情发展时进行重新检测。
基因组谱分析与下一代测序技术(NGS)的采用已证明,在转移性前列腺癌男性患者的肿瘤中存在多种多样的突变模式。1,2遗传测试可以确定哪些患者可以从PPAR抑制剂中受益,例如olaparib(Lynparza)和rucaparib(Rubraca),还可以确定其肿瘤对CPI更有反应的患者。这些亚型具有与DNA修复缺陷相关的突变3的共同特征,包括缺陷错配修复基因(dMMR)/高微卫星不稳定性(MSI-H),PD-1 T细胞受体及其配体(PD- L1),高肿瘤突变负担(TMB)和CDK12突变的肿瘤。
尽管CPI对普通患者的毒性比化疗低,但在许多研究中,它们并不具有良性,并且与治疗相关的死亡风险很小,但却是真正的风险,并且住院风险为10%到20%。它们也是昂贵的疗法,必须静脉注射(IV)。但是,我们认为应该慎重考虑何时和向谁推荐CPI (表),并将它们限制在基因组学表明有有意义的反应机会的患者中。
对CPI有反应的前列腺癌亚型
dMMR / MSI-H。与没有此类MMR缺陷的肿瘤相比,缺乏dMMR机制的肿瘤发生了超突变,并且来自这些其他突变的新抗原具有更高的免疫原性。鼓励使用NGS在所有晚期前列腺癌患者中寻找dMMR / MSI-H。Pembrolizumab(Keytruda)已获得FDA的全面批准,可用于在先前治疗中进展的dMMR / MSI-H前列腺癌患者。5一项在mCRPC中的初步研究表明,用培姆单抗和enzalutamide组合治疗的dMMR / MSI-H患者的临床反应,表明高的新抗原负荷可以预测对CPI的反应。
在随后的针对mCRPC的病例系列中,只有3.1%(32例患者)患有dMMR / MSI-H PC。在接受PD-1 / PD-L1治疗的11例患者中,有55%的前列腺特异性抗原(PSA)下降,而45%的患者可获得长达19个月的持久临床获益。
很明显,大多数前列腺癌患者无法从当前的CPI中受益,但是很明显,可以通过基因组检测确定可以从免疫疗法中受益的转移性去势抵抗性前列腺癌(mCRPC)的某些分子亚型。我们有许多好的新疗法可以治疗前列腺癌,但转移性疾病仍然无法治愈,将成为大多数患者的死亡原因。他们将死于前列腺癌,而不仅仅是死于前列腺癌。只要这仍然是对的,对前列腺癌的免疫疗法的兴趣仍然很高。
尽管对此的理想答案是让患者参加临床试验,但在某些情况下,非审判治疗是最佳的选择。接下来是我们对晚期前列腺癌患者的CPI评估方法。
下一代测序的作用
前列腺癌患者存在基因表达谱以及种系和体细胞突变的生物学差异。美国国家综合癌症网络指南现在建议对所有患有高危,极高危或转移性前列腺癌的男性进行种系检测。我们还对所有转移性疾病患者进行体细胞(肿瘤)检测,并在系统治疗的基础上,每当病情发展时进行重新检测。
基因组谱分析与下一代测序技术(NGS)的采用已证明,在转移性前列腺癌男性患者的肿瘤中存在多种多样的突变模式。1,2遗传测试可以确定哪些患者可以从PPAR抑制剂中受益,例如olaparib(Lynparza)和rucaparib(Rubraca),还可以确定其肿瘤对CPI更有反应的患者。这些亚型具有与DNA修复缺陷相关的突变3的共同特征,包括缺陷错配修复基因(dMMR)/高微卫星不稳定性(MSI-H),PD-1 T细胞受体及其配体(PD- L1),高肿瘤突变负担(TMB)和CDK12突变的肿瘤。
尽管CPI对普通患者的毒性比化疗低,但在许多研究中,它们并不具有良性,并且与治疗相关的死亡风险很小,但却是真正的风险,并且住院风险为10%到20%。它们也是昂贵的疗法,必须静脉注射(IV)。但是,我们认为应该慎重考虑何时和向谁推荐CPI (表),并将它们限制在基因组学表明有有意义的反应机会的患者中。
对CPI有反应的前列腺癌亚型
dMMR / MSI-H。与没有此类MMR缺陷的肿瘤相比,缺乏dMMR机制的肿瘤发生了超突变,并且来自这些其他突变的新抗原具有更高的免疫原性。鼓励使用NGS在所有晚期前列腺癌患者中寻找dMMR / MSI-H。Pembrolizumab(Keytruda)已获得FDA的全面批准,可用于在先前治疗中进展的dMMR / MSI-H前列腺癌患者。5一项在mCRPC中的初步研究表明,用培姆单抗和enzalutamide组合治疗的dMMR / MSI-H患者的临床反应,表明高的新抗原负荷可以预测对CPI的反应。
在随后的针对mCRPC的病例系列中,只有3.1%(32例患者)患有dMMR / MSI-H PC。在接受PD-1 / PD-L1治疗的11例患者中,有55%的前列腺特异性抗原(PSA)下降,而45%的患者可获得长达19个月的持久临床获益。
 PD-1 / PD-L1的过表达。开放标签的篮子1b期KEYNOTE-028试验每24周研究一次10毫克/公斤的派姆单抗静脉注射,持续24个月。其中包括245例mCRPC患者。PD-L1阳性35例(14%)。在接受Pembrolizumab的PD-L1阳性的35名患者中,有23名患者的总缓解率(ORR)为17%,其中稳定疾病的比例为35%,进行性疾病的比例为39%,中位缓解时间为13.5个月,中位总生存期为8个月。这些发现得到了KEYNOTE-199的确认,这是一项539期多西他赛难治性mCRPC患者每3周使用pembrolizumab 200 mg IV进行为期21个周期的2期试验。8该研究显示PD-L1在mCRPC中的过表达为32%,在8%中在原发性前列腺癌中。8在包括133名患者的PD-L1阳性队列中,ORR为7%,中位缓解时间(mDOR)为16.8个月,完全缓解(CR)为2位患者,中位总生存时间为9.5个月。
值得注意的是,探索PD-1 / PD-L1在前列腺癌中表达的研究使用了不同的技术和阈值,从而导致阳性率的高度可变。总而言之,这些综合结果表明,多达32%的晚期前列腺癌可能使用PD-L1途径逃避了免疫系统的检测。患有mCRPC和PD-L1亚型的患者可从单药pembrolizumab获得少量但有意义的且有时持久的获益。
高TMB。与病程较早的患者相比,mCRPC患者的TMB似乎更高。通常,具有较高TMB的肿瘤与dMMR相关。来自CHECKMATE 650试验(NCT029855957)的初步报告,使用ipilimumab(Yervoy)和nivolumab(Opdivo)联合使用,在TMB高的患者相比TMB低的患者(未报道TMB截止)。结果显示,未进行过化学疗法(60%对0%)和基于紫杉烷的化学疗法(50%对0%)后的ORR均为58%。
双等位基因CDK12突变。CDK12是一种涉及基因组稳定性的肿瘤抑制蛋白。10临床前研究表明,双等位基因CDK12突变与更高的新抗原,肿瘤浸润的淋巴细胞以及对CPI的更高敏感性有关。12,13最初的一项回顾性研究表明,在接受PD-1抑制剂作为四线至六线治疗的8例患者中,CPI敏感性较高。这些经过严格治疗的患者的PSA下降38%,超过50%,中位PFS为6.6个月。14这些结果在一项回顾性研究中得到了证实,该研究涉及46名CDK12患者突变(34个双等位基因突变)。在接受PD-1抑制剂治疗的5名患者中,有40%达到了PSA反应。
最后,一项较大的回顾性多中心研究包括60例患有体细胞功能丧失CDK12突变的前列腺癌患者。9例患者接受了PD-1抑制剂治疗(第5线至第6线使用PD-1抑制剂(5例使用pembrolizumab,4例使用nivolumab),其中33%的患者有PSA反应,中位PFS为5.4个月。16一项正在进行的前瞻性临床试验(NCT03570619)正在研究CDK12作为CPI在前列腺癌中使用的生物标志物的预测作用。
POLE和POLD突变。选择的POLE和POLD突变可产生与无MSI-H的很高TMB相关的肿瘤。在约2%的前列腺癌中发现了这些突变。已有报道,在对Pembrrolizumab的特殊应答者中有病例报告,其中记载了POLE V411L突变。同样,据报道,患有POLD1 D402N,MSH2突变和高TMB的患者对pembrolizumab的临床反应良好。
结论:
在我们的实践中,我们根据患者的肿瘤遗传特征积极地将患者分类到不同的治疗途径上。一小部分但有意义的患者将具有遗传畸变,这些遗传畸变可预测对CPI的反应,而那些幸运患者的结果可能是惊人的。我们尝试让患者尽可能多地参加免疫疗法试验。这些试验通常涉及现有药物的组合,但也可能涉及对mCRPC更有效的全新药物。
我们最近报道了对PT-112进行1期研究的中位先期治疗中位数为6.5行的患者的结果。在该试验中,接受PT-112治疗的10名患者的平均总生存期为15.1个月。我们也将PT-112与avelumab(Bavencio)结合使用,并据此进行研究。
有许多可能性尚待探索,我们需要找到一种将免疫疗法扩展到所有mCRPC患者的方法。同时,NGS可以识别最可能对CPI产生反应的患者,同时还可以识别携带遗传易感基因的患者和将从PARP抑制剂中获益的患者。
Gonzalez-Velez是亚利桑那州凤凰城梅奥诊所的血液学/肿瘤学研究员,而Bryce是亚利桑那州凤凰城梅奥诊所的医学副教授。
相关阅读你推荐:《免疫药联合奥拉帕尼能治疗前列腺癌吗?》
PD-1 / PD-L1的过表达。开放标签的篮子1b期KEYNOTE-028试验每24周研究一次10毫克/公斤的派姆单抗静脉注射,持续24个月。其中包括245例mCRPC患者。PD-L1阳性35例(14%)。在接受Pembrolizumab的PD-L1阳性的35名患者中,有23名患者的总缓解率(ORR)为17%,其中稳定疾病的比例为35%,进行性疾病的比例为39%,中位缓解时间为13.5个月,中位总生存期为8个月。这些发现得到了KEYNOTE-199的确认,这是一项539期多西他赛难治性mCRPC患者每3周使用pembrolizumab 200 mg IV进行为期21个周期的2期试验。8该研究显示PD-L1在mCRPC中的过表达为32%,在8%中在原发性前列腺癌中。8在包括133名患者的PD-L1阳性队列中,ORR为7%,中位缓解时间(mDOR)为16.8个月,完全缓解(CR)为2位患者,中位总生存时间为9.5个月。
值得注意的是,探索PD-1 / PD-L1在前列腺癌中表达的研究使用了不同的技术和阈值,从而导致阳性率的高度可变。总而言之,这些综合结果表明,多达32%的晚期前列腺癌可能使用PD-L1途径逃避了免疫系统的检测。患有mCRPC和PD-L1亚型的患者可从单药pembrolizumab获得少量但有意义的且有时持久的获益。
高TMB。与病程较早的患者相比,mCRPC患者的TMB似乎更高。通常,具有较高TMB的肿瘤与dMMR相关。来自CHECKMATE 650试验(NCT029855957)的初步报告,使用ipilimumab(Yervoy)和nivolumab(Opdivo)联合使用,在TMB高的患者相比TMB低的患者(未报道TMB截止)。结果显示,未进行过化学疗法(60%对0%)和基于紫杉烷的化学疗法(50%对0%)后的ORR均为58%。
双等位基因CDK12突变。CDK12是一种涉及基因组稳定性的肿瘤抑制蛋白。10临床前研究表明,双等位基因CDK12突变与更高的新抗原,肿瘤浸润的淋巴细胞以及对CPI的更高敏感性有关。12,13最初的一项回顾性研究表明,在接受PD-1抑制剂作为四线至六线治疗的8例患者中,CPI敏感性较高。这些经过严格治疗的患者的PSA下降38%,超过50%,中位PFS为6.6个月。14这些结果在一项回顾性研究中得到了证实,该研究涉及46名CDK12患者突变(34个双等位基因突变)。在接受PD-1抑制剂治疗的5名患者中,有40%达到了PSA反应。
最后,一项较大的回顾性多中心研究包括60例患有体细胞功能丧失CDK12突变的前列腺癌患者。9例患者接受了PD-1抑制剂治疗(第5线至第6线使用PD-1抑制剂(5例使用pembrolizumab,4例使用nivolumab),其中33%的患者有PSA反应,中位PFS为5.4个月。16一项正在进行的前瞻性临床试验(NCT03570619)正在研究CDK12作为CPI在前列腺癌中使用的生物标志物的预测作用。
POLE和POLD突变。选择的POLE和POLD突变可产生与无MSI-H的很高TMB相关的肿瘤。在约2%的前列腺癌中发现了这些突变。已有报道,在对Pembrrolizumab的特殊应答者中有病例报告,其中记载了POLE V411L突变。同样,据报道,患有POLD1 D402N,MSH2突变和高TMB的患者对pembrolizumab的临床反应良好。
结论:
在我们的实践中,我们根据患者的肿瘤遗传特征积极地将患者分类到不同的治疗途径上。一小部分但有意义的患者将具有遗传畸变,这些遗传畸变可预测对CPI的反应,而那些幸运患者的结果可能是惊人的。我们尝试让患者尽可能多地参加免疫疗法试验。这些试验通常涉及现有药物的组合,但也可能涉及对mCRPC更有效的全新药物。
我们最近报道了对PT-112进行1期研究的中位先期治疗中位数为6.5行的患者的结果。在该试验中,接受PT-112治疗的10名患者的平均总生存期为15.1个月。我们也将PT-112与avelumab(Bavencio)结合使用,并据此进行研究。
有许多可能性尚待探索,我们需要找到一种将免疫疗法扩展到所有mCRPC患者的方法。同时,NGS可以识别最可能对CPI产生反应的患者,同时还可以识别携带遗传易感基因的患者和将从PARP抑制剂中获益的患者。
Gonzalez-Velez是亚利桑那州凤凰城梅奥诊所的血液学/肿瘤学研究员,而Bryce是亚利桑那州凤凰城梅奥诊所的医学副教授。
相关阅读你推荐:《免疫药联合奥拉帕尼能治疗前列腺癌吗?》
用药温馨提示:当您服用此药物时,需定期接受医疗专业人士的检查,以便随时针对其药效、副作用等情况进行监测。本网站所包含的信息旨在为患者提供帮助,不能代替医学建议和治疗。
药品价格查询,专业药品查询网站,药品说明书查询,药品比价 » 前列腺癌如何进行免疫检查点抑制剂治疗
药品价格查询,专业药品查询网站,药品说明书查询,药品比价 » 前列腺癌如何进行免疫检查点抑制剂治疗










